研究ハイライト
エステル化合物と有機ホウ素化合物を切ってつなげる新反応 〜ニッケル触媒が安定なエステル化合物を活性化〜
名古屋大学トランスフォーマティブ生命分子研究所(ITbM)、JST戦略的創造研究推進事業ERATO伊丹分子ナノカーボンプロジェクト、名古屋大学大学院理学研究科の伊丹健一郎教授、山口潤一郎准教授、武藤慶(大学院生)および米国エモリー大学のムサエフ・ジャマラッディン教授は、エステル化合物と有機ホウ素化合物(有機ボロン酸)を切ってつなげる画期的な新反応の開発に成功しました。 今回開発した手法によって、通常、鈴木--宮浦カップリング反応(ノーベル化学賞)に用いられる有機ハロゲン化物の代わりに、多様に存在するエステル化合物を用いることが初めて可能になりました。 本手法のもうひとつの利点は、安価なニッケル錯体を触媒に用いることにあります。 医農薬や有機エレクトロニクス材料の安価かつ新しい工業的プロセスの開発につながることが期待されます。 本研究成果は、ネイチャー・コミュニケーションズ誌のオンライン版で2015年6月29日に公開されました。
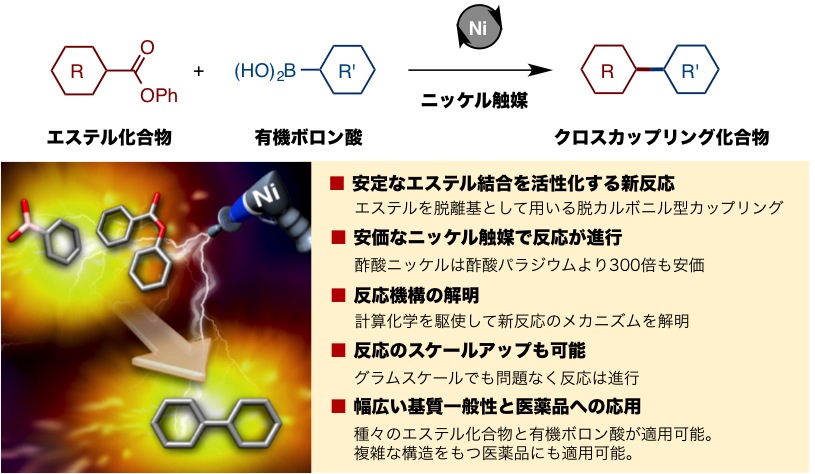
概要:
鈴木--宮浦カップリング反応は、通常パラジウム触媒の存在下で、カップリング剤として有機ホウ素化合物と有機ハロゲン化物を連結する反応です。両カップリング剤を用意すれば、容易に分子と分子を連結できることから、最も信頼性の高い合成化学手法として医農薬や有機エレクトロニクス材料、液晶材料の合成に用いられています。その結果、クロスカップリング反応が2010年のノーベル化学賞の受賞対象となったことは記憶に新しいことでしょう。一方で、クロスカップリング反応をより実用的にする試みが世界中で展開されています。有機ハロゲン化物の使用により反応後に環境へ悪影響を与える金属ハロゲン化物を排出してしまう「ハロゲン問題」を解決する代替カップリング剤の開発や安価かつ高活性な新触媒の開発などです。例えば、鈴木−宮浦カップリング反応においては、有機ハロゲン化物の代替カップリング剤として、有機ジアゾニウム塩・有機アンモニウム塩・フェノール誘導体・チオフェノール誘導体などを使い、パラジウムもしくはニッケル触媒により反応を進行させる様々な「鈴木--宮浦カップリング型反応」が報告されています(図1)。今回、伊丹教授らの研究チームは有機ハロゲン化物の代替カップリング剤として入手容易で安定な「エステル化合物」に着目し、これを有機ホウ素化合物と連結させる反応の開発に挑戦しました。
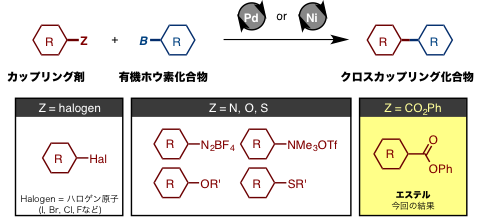
エステル化合物は、有機ハロゲン化物を用いる場合と比較し、ハロゲン化物由来の廃棄物を排出せず、カルボン酸誘導体として極めて多種類のものが市販品として手に入ります。さらに、エステル基は古くから用いられるヘテロ環合成法でヘテロ芳香環を合成する場合に必要な官能基であり、それらを直接用いて結合をつくることが可能となれば合成工程の短縮にも繋がります。しかしながら、エステルは安定な官能基であり、これをカップリング剤として用いることはほとんどできませんでした。
反応条件を種々検討したところ、非常に安価な触媒(酢酸ニッケル、トリブチルホスフィン、炭酸ナトリウム)を用いることでエステル基が脱離基となり種々の有機ボロン酸と反応することを見出しました(図2)。
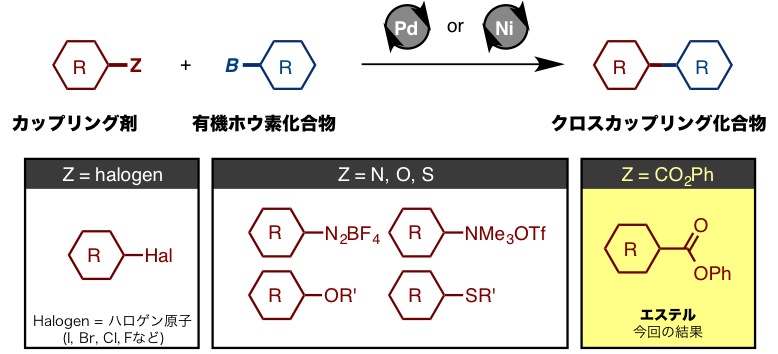
本法は従来法と比較して、多様に存在するカルボン酸誘導体(エステル)をそのまま脱離基として使えることが最大の特徴です。また、安価なニッケル錯体を触媒に用いることも大きな魅力であり、触媒前駆体の酢酸ニッケルは、鈴木--宮浦カップリングの触媒前駆体として頻繁に用いられる酢酸パラジウムに比べて、その価格は300倍も安価です。さらに本反応は、幅広い基質一般性を示すとともに、複雑な構造をもつ医薬品にも適用できます(図3)。この反応は、特にヘテロ芳香環エステル化合物のカップリングに威力を発揮し、ハロゲン化物を用いたカップリングでは、多段階を要する、もしくは合成困難な化合物の合成が容易になりました。極めて高い合成的実用性を有していると言えます。また、反応はグラムスケールでも問題なく進行することから反応のスケールアップも可能です。
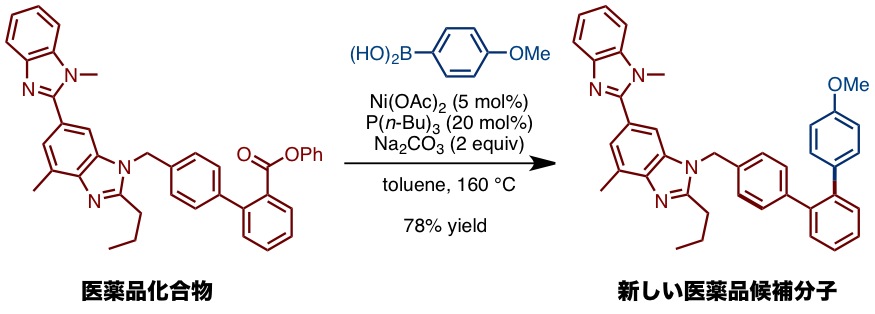
入手容易かつ安定なエステル化合物がカップリング剤として使えるという今回の知見は、今後カルボン酸誘導体を鈴木--宮浦カップリング型のみでなく様々なクロスカップリング反応の代替カップリング剤として活用できる可能性を示しています。クロスカップリング反応は現在のファインケミカルを生み出す化学工業の必須合成技術であり、今回開発された次世代型カップリング反応は医農薬や有機エレクトロニクス材料の安価かつ新しい工業的プロセスの開発につながることが期待されます。
論文情報:
"Decarbonylative organoboron cross-coupling of esters by nickel catalysis" by Kei Muto, Junichiro Yamaguchi, Djamaladdin G. Musaev & Kenichiro Itami is published online on June 29, 2015 in Nature Communications.
リンク:
- プレスリリース
- Alpha Galileo JP「エステル化合物と有機ホウ素化合物を切ってつなげる新反応 〜ニッケル触媒が安定なエステル化合物を活性化〜」(2015.06.29)
- EurekAlert! JP「エステル化合物と有機ホウ素化合物を切ってつなげる新反応」(2015.06.29)
- 日本の研究.com「エステル化合物と有機ホウ素化合物を切ってつなげる新反応-ニッケル触媒が安定なエステル化合物を活性化-」(2015.07.01)
- Nature注目の論文「ニッケル触媒によるエステルの脱カルボニル型有機ホウ素クロスカップリング反応ブックマーク」(2015.09.08)

伊丹健一郎教授: http://www.itbm.nagoya-u.ac.jp/ja_backup/members/k-itami/
山口潤一郎准教授: http://www.itbm.nagoya-u.ac.jp/ja_backup/members/j-yamaguchi/


関連記事・報道:
2015-06-29

