触媒的炭素-水素結合活性化による 含七員環ナノカーボン合成 ~容易に合成、高い溶解性・凝集状態で強まる発光特性を確認~
【ポイント】
・パラジウム触媒を用いた炭素-水素結合活性化により高効率で七員環骨格を構築
・様々な含七員環ナノカーボンやヘテロ多環芳香族炭化水素注1)の合成が可能
・入手容易な出発物質から一つのフラスコで一挙に複数環構築が可能
・量子化学計算による反応機構の解明
・湾曲した七員環骨格による高い溶解性、凝集状態での発光特性の発現【研究概要】
国立大学法人東海国立大学機構 名古屋大学大学院理学研究科の伊藤 英人 准教授、名古屋大学トランスフォーマティブ生命分子研究所(WPI-ITbM)の伊丹 健一郎 教授、山田 圭悟 博士後期課程学生らは、効率的かつ迅速な「パラジウム触媒を用いた含七員環ナノカーボンの合成法」の開発に成功しました。
グラフェンなどの六員環(ベンゼン)骨格の炭素材料では、非六員環(五・七・八員環)に起因した非六員環ナノカーボンが存在し、さまざまな物理的性質を示すことが知られていますが、「含七員環ナノカーボン」の効率的な合成法が限られていました。
本研究では、パラジウム触媒を用いた炭素-水素結合活性化反応を伴うカップリング反応注2)により、含七員環ナノカーボンの効率的な新規合成法を実現しました。この方法では、ブロモ基をもつ芳香環連結分子を原料として、様々な骨格をもつ幅広い含七員環ナノカーボンのみならず、ヘテロ原子注3)を含む多環芳香族炭化水素を良好な収率で得ることに成功しました。また、ロジウム触媒およびパラジウム触媒を組み合わせた逐次的な反応によって、入手容易な原料から各々2つの六員環と七員環を一挙に構築でき、これまでにない複雑な骨格をもつナノカーボンの合成も可能となりました。量子化学計算によって詳細な触媒反応機構が明らかとなり、七員環合成法の有用性が確認されました。さらに、合成された含七員環ナノカーボンは、湾曲した骨格により幅広い有機溶媒への高い溶解性を示すと同時に、固体凝集状態で強まる発光特性などのユニークな性質を有していることが分かりました。このような特性は構造有機化学、および有機EL材料や分子デバイスなどの材料科学の分野への応用が期待されます。 本研究は広範な含七員環ナノカーボンの合成の新しい指針となることが予想され、また合成した分子骨格としても新たな機能性分子としての応用展開が期待されます。
本研究成果は、2023年11月16日付ドイツ化学会誌「Angewandte Chemie International Edition」のオンライン速報版に掲載されました。
【研究の背景】
一般に、ベンゼンなどの六員環骨格からなる多環芳香族炭化水素化合物やそれらの連結分子は広義でナノカーボンと呼ばれています。一方、五・七・八員環を含むナノカーボンは「非六員環ナノカーボン」と呼ばれ、その湾曲構造と芳香族・反芳香族性/導電性/光物性などのユニークな物性により、構造有機化学や材料科学など様々な分野で近年大きな注目を集めています。
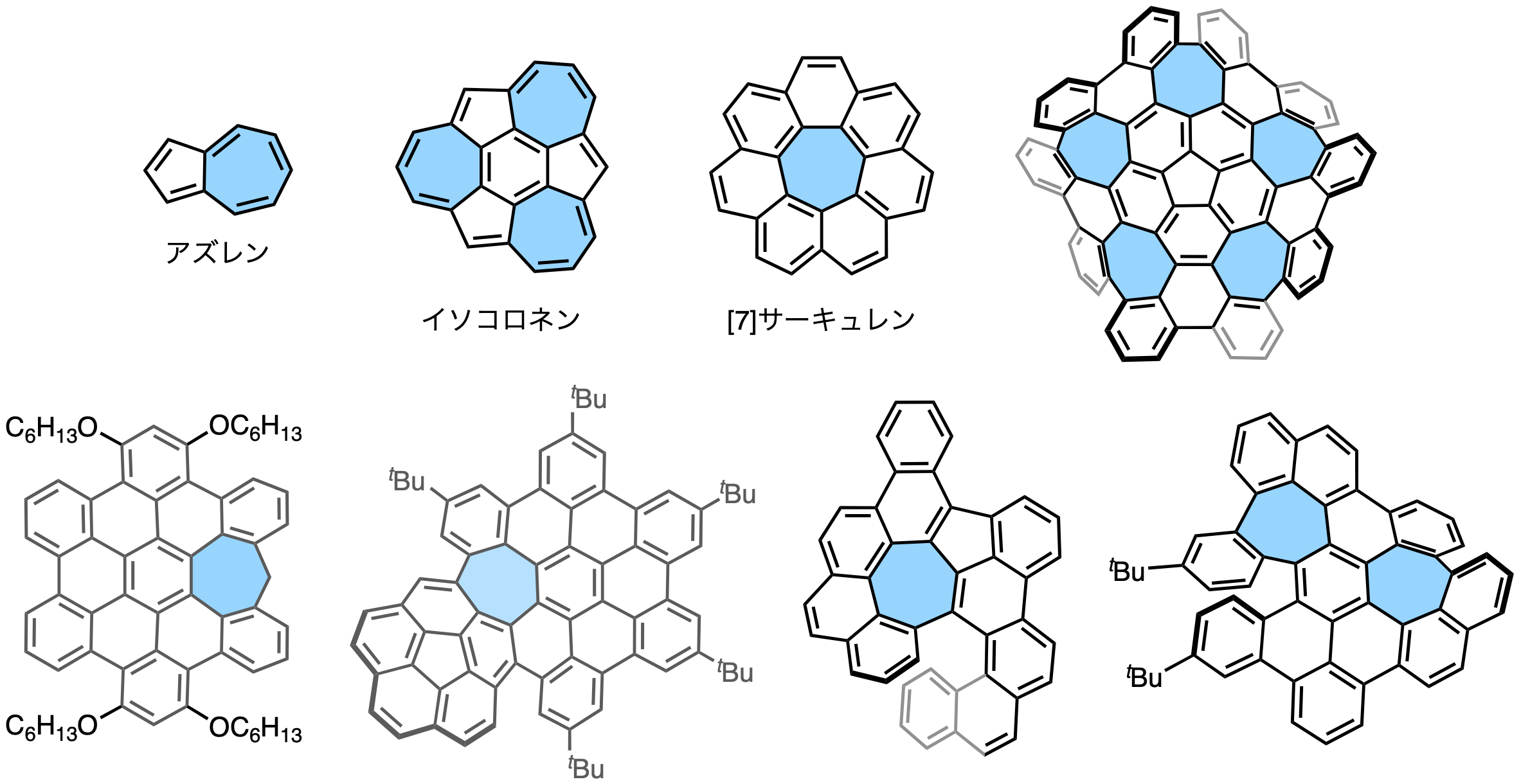
中でも、アズレン、イソコロネン、[7]サーキュレン、ワープドナノグラフェンなどの含七員環ナノカーボンやその誘導体は、魅力的な合成ターゲットです。これらの化合物は負に湾曲した七員環部位に由来するトロピリウムカチオンの安定性により、対応する含六員環ナノカーボンに比べて高いHOMOや、五・六・七員環の縮環様式に由来する芳香族性/反芳香族性を特徴としています(図1)。
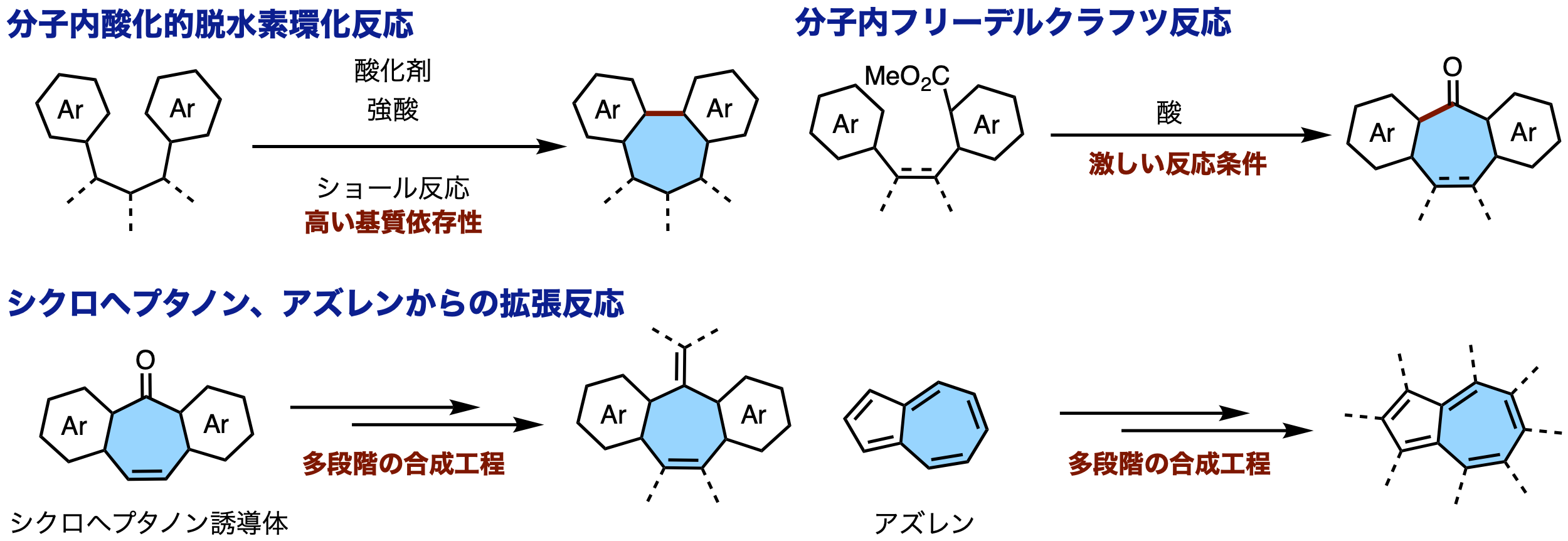
多数の報告がある含五員環・六員環ナノカーボンとは対照的に、七員環の形成はエントロピーやエンタルピーの観点から本質的に困難であり、含七員環ナノカーボンの合成に適用できる方法も限られています。上記の含七員環ナノカーボンの合成例は、基質依存性が高い酸化的脱水素環化反応(ショール反応) 注4)や、激しい反応条件を要する分子内Friedel-Crafts反応、または数少ない市販の含七員環化合物からの誘導体化がほとんどです(図2)。そのため、これまで多種多様な構造をもつ含七員環ナノカーボンの自在合成法は確立されているとは言えず、新たな効率的七員環骨格構築法の開発が望まれていました。
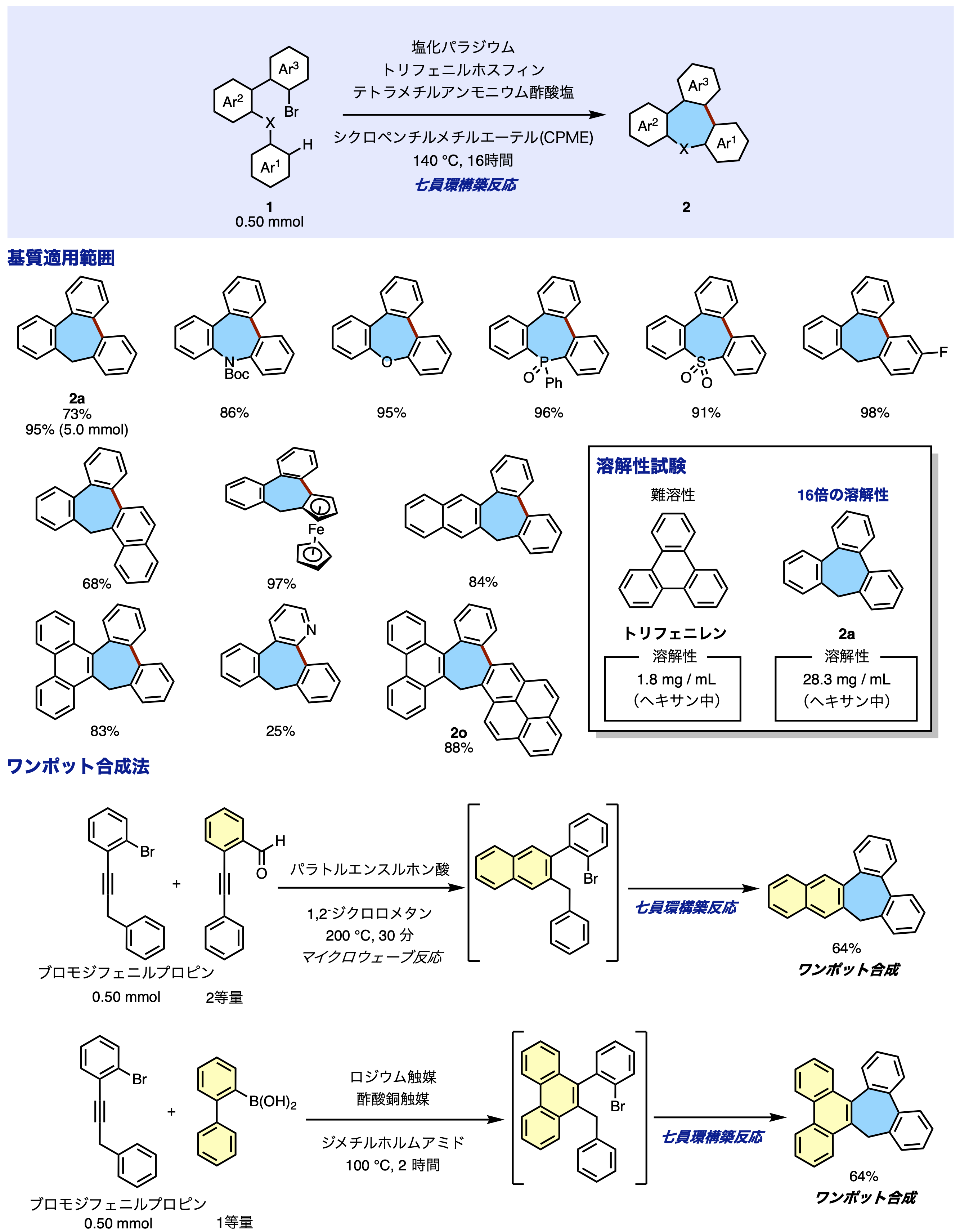
研究グループは、パラジウム触媒を用いた分子内炭素-水素結合(C-H結合)活性化反応による含七員環ナノカーボンの効率的な合成法を報告しました(図3)。ベンジルブロモビフェニル誘導体および類縁体1に対し、パラジウム触媒を作用させることで分子内カップリングを可能とし、分子内Ar-H/Ar-Brカップリングによる効率的な七員環形成が可能となりました。種々の条件検討の結果、様々なヘテロ原子を有する含七員環ナノカーボンやフェロセン、ナフタレン、フェナントレン、ピレンなどが縮環したナノカーボンにおいても良好に反応が進行することが明らかとなりました。
さらに室温(23℃)下、ヘキサン中で含七員環化合物2aと平面六員環構造をもつトリフェニレンの溶解度を測定し比較しました。トリフェニレンのような高い平面性をもつナノカーボンは一般に低溶解性です。結果として、含七員環化合物である2aは、トリフェニレンよりも16倍高い溶解度を示しました。
さらに本反応では、より入手容易な出発物質であるブロモジフェニルプロピンからDiels-Alder型反応もしくはロジウム触媒を用いた六員環形成反応後にパラジウム触媒を連続的に作用させることで、単一フラスコ(ワンポット)で簡便かつ容易に六員環と七員環を構築することに成功しました。これらのワンポット反応の成功例は、用いる原料の組み合わせを調整するだけで、他の様々な骨格をもつ含七員環ナノカーボンを迅速かつ効率的に構築できる可能性を示しています。
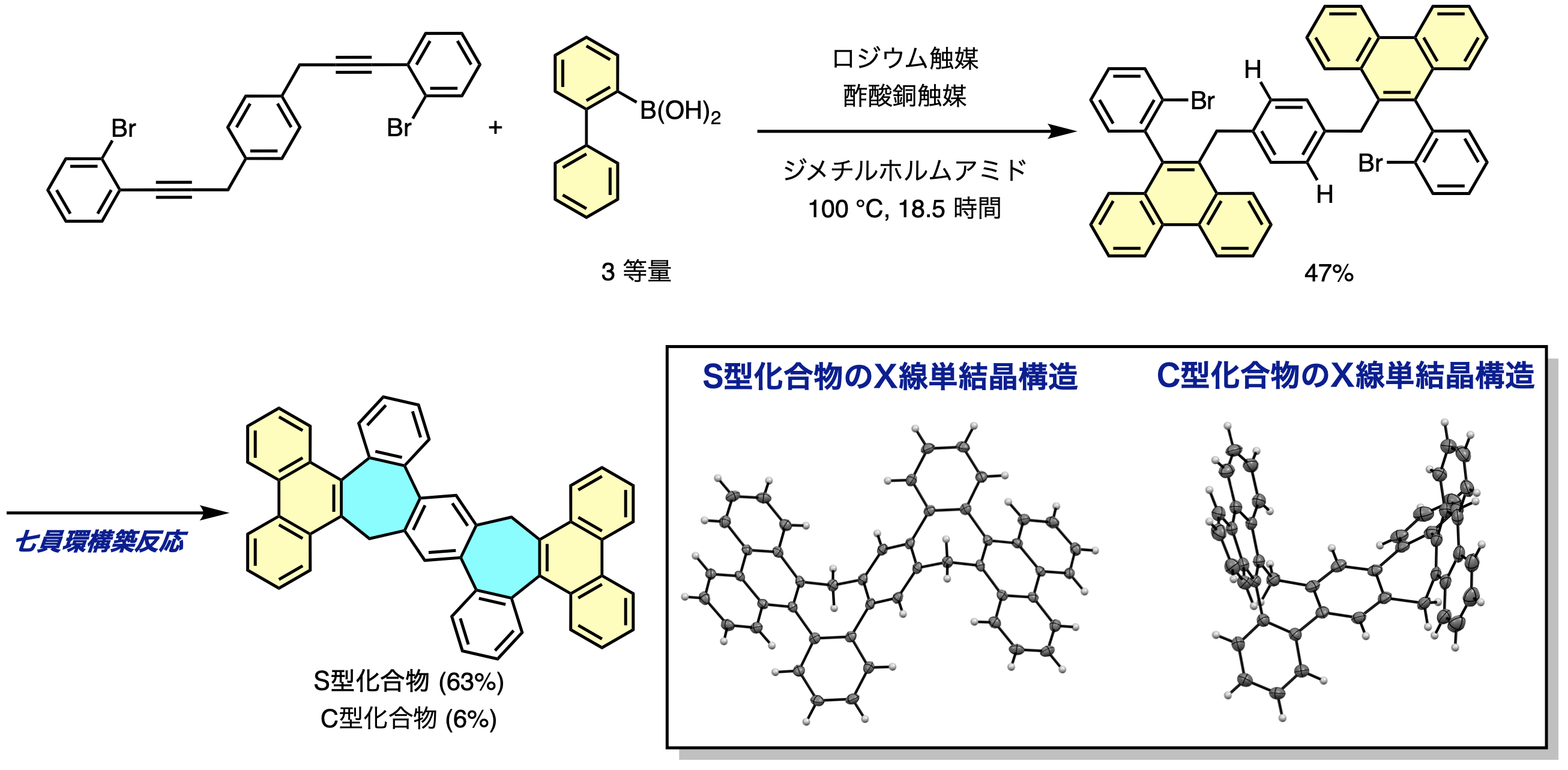
より大きな含七員環ナノカーボンを簡便に作るために、アルキン化合物とアリールボロン酸を原料に、ロジウム触媒による二箇所同時の六員環形成と、続くパラジウム触媒による二箇所同時の七員環骨格の構築を行いました。この反応は、二段階の反応を同一フラスコで実施できる「ワンポット反応」と呼ばれており、結果として9個の六員環と2個の七員環を含む新しいナノカーボンを69%の高い収率で得ることができました。
通常、六員環だけからなるナノカーボンは平面構造であり異性体が存在しませんが、驚くことにこの含七員環ナノカーボンには、S字型とC字型の2つの異なる安定な配座異性体があることがX線単結晶構造解析によって判明し、これらの形は2つの七員環の湾曲構造に起因していることが明らかとなりました。この特徴は、含七員環ナノカーボンの構造と性質を理解する上で重要な発見です。
また、本反応の反応機構は、密度汎関数(DFT)法による量子化学計算に基づき、以下の機構で反応が進行していることが示唆されました。(1) Pd(0)種へのブロモアレーン(Ar-Br)の酸化的付加、(2) 協奏的メタル化-脱プロトン化(CMD)機構を介した炭素-水素結合活性化による八員環パラダサイクルの生成、(3)還元的脱離による生成物の生成です。実験的にはエントロピー的に有利な含五員環化合物(六員環の中間体を経由)がほとんど検出されず、七員環を含む化合物のみが生成されることが明らかになり、もっとも難しい七員環形成段階(CMD過程)の活性化障壁が31kcal/molと、この律速段階であることが明らかになりました。
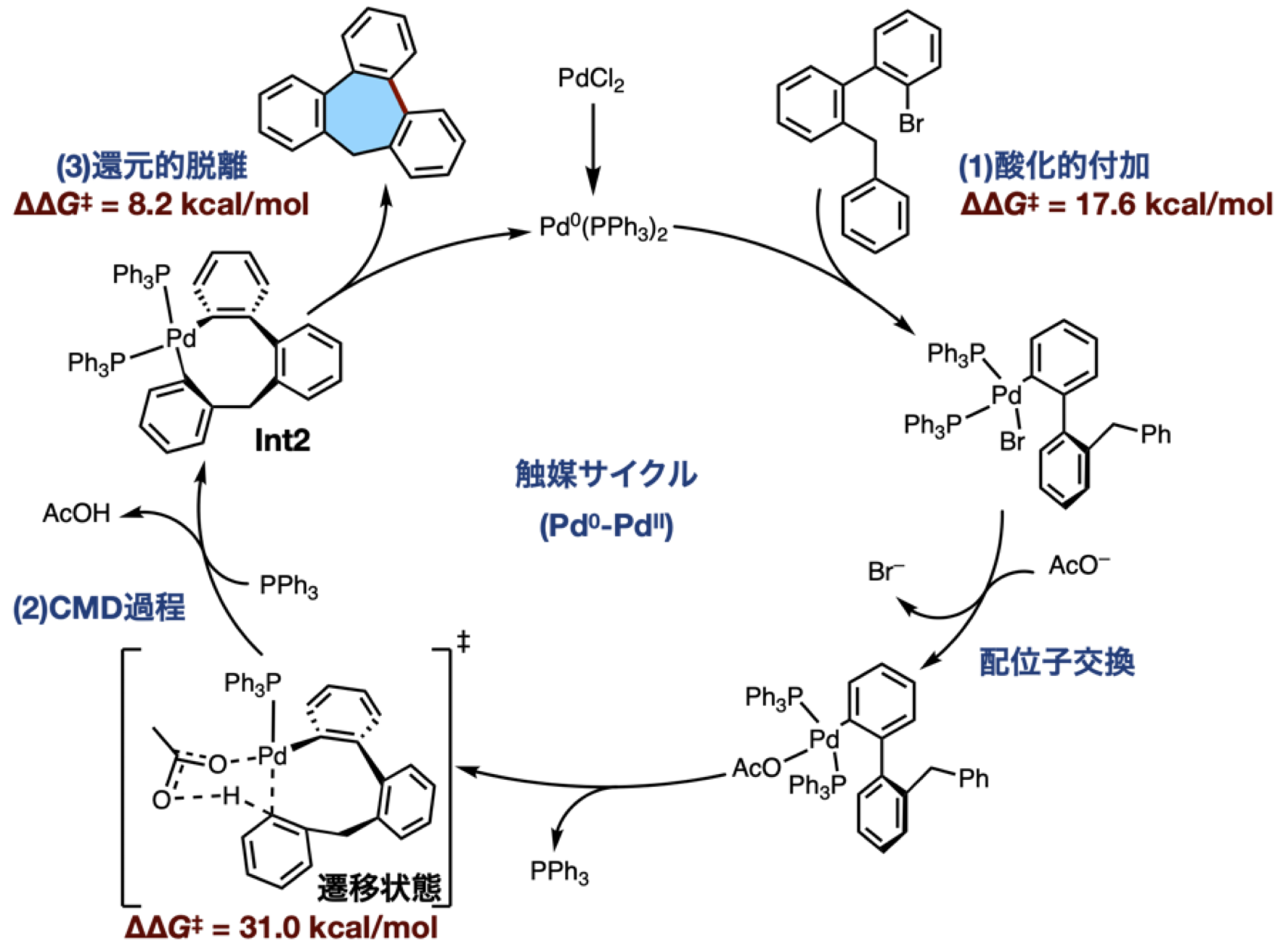
図5:本反応の反応機構。CMD過程の活性化エネルギーが最も高く、本反応の律速段階であることが分かる。
最後に、紫外可視吸収測定および蛍光測定において、含七員環ナノカーボンのほとんどは、溶媒のテトラヒドロフラン(THF)中で弱い青色蛍光を示すことが分かりました(図6)。しかし、この溶液中に対して水を加えるにつれて、化合物の蛍光強度が増加する現象が見られました。これは、水の添加によって固体として凝集した化合物がより強い発光を示す、「凝集誘起発光(AIE)」と呼ばれる現象です。特にピレン骨格を含む化合物2oは、水の割合が0%から75%の範囲ではAIEによる発光増強が観測されましたが、水の割合が90%から99%になるとエキシマー発光が観測され、約60%の大きな蛍光量子収率を示しました。AIE発光とエキシマー発光の両方を示す化合物は珍しく、完全に芳香族化された含六員環ナノカーボンではほとんど観察されない特性です。
【まとめと今後の展開】
本研究ではパラジウム触媒を用いた炭素-水素結合活性化反応により、一般的で効率的な七員環形成反応を開発しました。本手法は広い基質適用範囲を示し、ヘテロ元素を含むものや複雑な縮環形式の含七員環化合物を高い効率で合成することができました。また、本反応を用いて入手容易な出発物質から七員環をワンポットで構築する方法も開発しました。量子化学計算により詳細な反応機構を明らかにするとともに、合成した含七員環化合物の湾曲構造に起因した高い溶解性や特殊な発光特性を明らかにしました。本手法の開発により、機能をもった新しい含七員環ナノカーボン材料を作るための新たな道が開かれたと考えられます。
【付記】
本成果は、以下の事業・共同利用研究施設による支援を受けて行われました。
戦略的創造研究推進事業 総括実施型研究(ERATO)(JPMJER1302)
研究プロジェクト:「伊丹分子ナノカーボンプロジェクト」
研究総括:伊丹 健一郎
研究期間:2013年10月~2020年3月
日本学術振興会 科学研究費補助金 特別推進研究(JP19H05463)
研究プロジェクト:「未踏分子ナノカーボンの創製」
研究代表者:伊丹 健一郎
研究期間:2019年4月~2022年3月
日本学術振興会 科学研究費補助金 基盤研究B(JP20K21192)
研究プロジェクト:「芳香族性制御によるポストナノカーボン合成化学」
研究総括:伊藤 英人
研究期間:2021年4月~2022年3月
戦略的創造研究推進事業(CREST)(JPMJCR19R1)
研究プロジェクト:「レドックスメカノケミストリーによる固体有機合成化学」
研究総括:伊藤 肇
主たる共同研究者:伊藤 英人
研究期間:2019年10月~2022年3月
公益財団法人 立松財団 一般研究助成
研究プロジェクト:「ナノカーボンの多様性指向型精密有機合成」
研究者代表者:伊藤 英人
研究期間:2023年8月~2024年9月
公益財団法人 近藤記念財団 研究助成
研究プロジェクト:「新炭素材料創出を目指したナノカーボンラダーポリマーの合成」
研究者代表者:伊藤 英人
研究期間:2022年10月~2024年9月
公益財団法人 野口研究所 野口遵研究助成金
研究プロジェクト:「Hetero-APEX反応の開発と新奇ヘテロ多環芳香族化<合物の迅速合成」
研究者代表者:伊藤 英人
研究期間:2020年4月~2022年3月
計算科学研究センター(Research Center for Computational Science) 施設利用
研究代表者:伊藤 英人
研究期間:2021年4月~2024年3月
課題番号:21-IMS-C070, 22-IMS-C069, 23-IMS-061
京都大学化学研究所スーパーコンピュータシステム 施設利用
研究代表者:伊藤 英人
研究期間:2022年10月~2023年3月
【用語説明】
注1)多環芳香族炭化水素:
ベンゼンやナフタレンよりも多くの芳香環をもつ芳香族炭化水素の総称であり、比較的小さな分子にはアントラセン、フェナントレン、ピレン 、ペリレン、コロネンなどの慣用名がある。英語略称名でPAHとも呼ばれる。
注2)カップリング反応:
パラジウム触媒などを用い、芳香族化合物同士を結合させる反応。鈴木・根岸・Heckらに与えられた2010年のノーベル化学賞の対象反応としても有名であり、1970年代から主に日本で盛んに研究されてきた。
注3)ヘテロ原子:
一般的にヘテロ原子は炭素や水素以外の原子を指す。特に有機化学の分野では慣用的に炭素と水素を除く非金属原子がヘテロ原子と呼ばれている。例えば酸素(O)、窒素(N)、硫黄(S)、リン(P)などがヘテロ原子に該当する。
注4)酸化的脱水素環化反応(ショール)反応:
ベンゼン環が連結した化合物に対して、塩化鉄(III)などを用いると水素原子の脱離を伴いながら環化して平面構造をもつ多環芳香族炭化水素が合成できる反応全般を指す。1910年、Schollらによって初めて報告された反応であり、現在ではナノグラフェン合成に欠かせない反応の一つとなっている。
Information
| 論文タイトル | Synthesis of Heptagon-Containing Polyarenes by Catalytic C−H Activation |
|---|---|
| 著者 | 山田 圭悟、Iain A. Stepek、松岡 和、伊藤 英人*、伊丹 健一郎*(*は責任著者) |
| 雑誌名 | Angewandte Chemie International Edition |
| DOI | 10.1002/anie.202311770 |
| 発行年月 | 2023年11月 |
