水素結合形成と青色光によって発生する 窒素ラジカル触媒の開発 ~分子を無駄なく思い通りに変換する合成技術の拡充に期待~
【本研究のポイント】
・分子内にカチオンとアニオンをもつ新しい分子性の光触媒を設計
・光励起によって発生する窒素ラジカルを触媒として利用することに成功
・水素結合を形成することで活性種として働く三重項励起種が効率的に発生
・青色光をエネルギー源として安定な炭素-水素結合を効率的に変換
【概要】
名古屋大学トランスフォーマティブ生命分子研究所(WPI-ITbM)・大学院工学研究科の大井 貴史 教授、大松 亨介 特任准教授†(現 慶應義塾大学理工学部 教授)、森 宗一郎 工学部学生†、山口 理恵 技術補佐員、鈴木 隆平 博士、名古屋大学WPI-ITbM・大学院理学研究科の柳井 毅 教授、仙頭 志音 博士前期課程学生、およびミュンスター大学(ドイツ)のOlga García Mancheño(オルガ・ガルシア・マンチェーニョ)教授、Lukas-Maximilian Entgelmeier(ルーカス マキシミリアン・エントゲルマイヤー)博士後期課程学生らの研究グループは、青色光の照射下で高い反応性を発現する新しい分子性の光触媒を開発しました。
研究グループは、アクリジニウムカチオン注1)とアミデートアニオン注2)が窒素-窒素結合でつながった分子を新たに設計しました。この分子は、青色光を吸収して励起注3)し、分子内での1電子移動によって生成する窒素ラジカル(アミジルラジカル)注4)を活性種とし、有機化合物の炭素-水素結合から水素原子を引き抜いて炭素ラジカル注4)を発生させる力を備えた光触媒として働きます。アミジルラジカルが水素原子を引き抜く力は非常に優れているため、通常はほとんど反応しないような安定な炭素-水素結合の変換も可能になる点が特徴です。また、触媒分子が溶媒として用いるヘキサフルオロイソプロパノールと水素結合を形成することが、光触媒としての優れた機能を発揮する上で不可欠であることを理論計算によって明らかにしました。
本研究成果は、2024年6月22日付ドイツ化学雑誌「Angewandte Chemie International Edition」電子版に掲載されました。
(† は研究当時)
【研究背景と内容】
有機化合物には炭素-水素結合が数多く含まれており、この結合から水素原子を引き抜いて炭素ラジカルを発生させる反応は、多種多様な化合物を無駄なく変換できる優れた合成化学技術です。特に、光励起によって発生するヘテロ原子のラジカルを活性種とするラジカル触媒を利用して水素原子を引き抜く方法は、温和な条件で効率的に反応を促進できるため、大きな注目を集め、盛んに研究されています。
水素原子引き抜きの成否は、炭素-水素結合の結合解離エネルギー注5)や電子的な性質等の複数の要因によって決まるため、ラジカル触媒を用いれば、どの炭素-水素結合からでも水素原子を引き抜けるわけではありません。すなわち、水素原子の引き抜き反応を進行させる上で重要なポイントは、対象となる炭素-水素結合に応じて、適切なラジカル触媒を用いることです。しかし、これまでに開発または発見されてきた触媒は酸素ラジカルと硫黄ラジカルを活性種とするものに限定されており、実現できる反応も自ずと限られていました。一方、窒素ラジカルは分子の構造を変えやすく、しかも高い反応性を発現しますが、窒素ラジカルの発生自体が困難であり、水素原子の引き抜きを担う光触媒として利用することに成功した例はありませんでした。
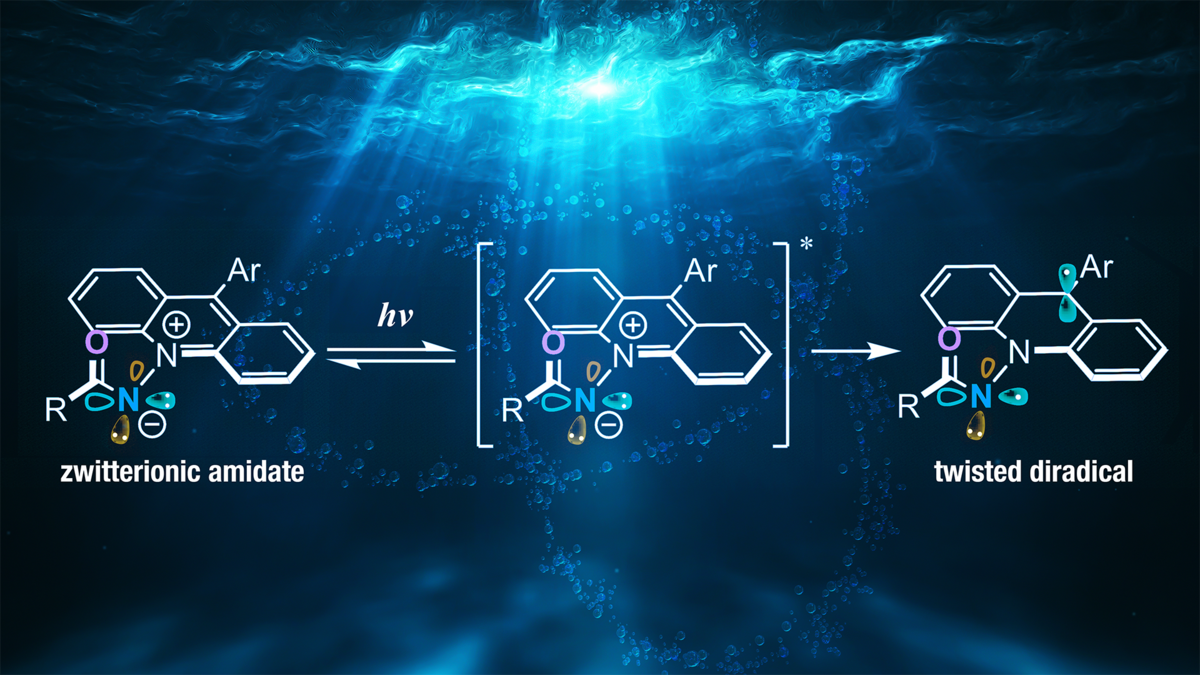
このような背景を踏まえて研究グループは、触媒の光励起を起点とする分子内での電子移動によって窒素ラジカルを発生させるという戦略を考えました。その実現のために、光レドックス触媒注6)として知られているアクリジニウムカチオンにアミデートアニオンをつないだ「双性イオン型アクリジニウムアミデート」を設計しました(図1)。この分子が青色光を吸収すると、アミデートアニオン上に分布する軌道からアクリジニウムカチオン上の軌道へ1電子が移動し、反応性の高い窒素ラジカルであるアミジルラジカルと安定なアクリジニルラジカルからなるジラジカルに変化することで、水素原子の引き抜きを担う光触媒として機能するのではないかという仮説を立てました。
実際、合成した双性イオン型アクリジニウムアミデートを光触媒として用いることで、シクロヘキサンのような安定な炭化水素化合物からの水素原子の引き抜きと、発生した炭素ラジカルのオレフィンへの付加反応を青色光の照射下で進行させ、アルキル化反応を効率的に行うことに成功しました(図1)。また、溶媒としてヘキサフルオロイソプロパノールを利用すると、反応の効率が飛躍的に向上することを発見しました。さらに、この現象の本質を理論計算によって精査し、触媒のアミデートアニオン部位とヘキサフルオロイソプロパノールが水素結合を形成することで、水素原子の引き抜きに関与する三重項励起種が発生しやすくなることを明らかにしました。
【成果の意義】
本研究では、反応性の高いアミジルラジカルを光励起によって効率的に発生させることができる分子の設計を提案し、その有効性を実証することに成功しました。新たに設計したアクリジニウムアミデートは分子の構造を容易に変更できるという特徴をもち、光触媒としての性質を細かく調節することも可能です。
今後、本触媒を活用することで、炭素-水素結合に限らず、様々な結合を標的とした化学反応の開発や、分子設計の自由度を活かした新たな機能の付与を目指す研究を広く展開することができ、入手容易な有機分子を無駄なく思い通りに変換するための合成技術の拡充につながると期待できます。
【付記】
本研究は、主に日本学術振興会 科学研究費助成事業(学術変革領域A)「炭素資源変換を革新するグリーン触媒科学」(2023〜2027年度)および(国際協働研究加速基金)「動的元素効果デザインによる未踏分子機能の探究」(2022〜2029年度)の支援のもとで行われたものです。
【用語説明】
注1)アクリジニウムカチオン:
窒素原子を含む芳香族化合物であるアクリジンが、窒素原子のプロトン化やアルキル化等を起こしてプラスの電荷をもった化合物。
注2)アミデートアニオン:
アミドの脱プロトンによって生じるアニオンの総称。アミドはC(=O)N配列をもつ化合物(Cは炭素原子、Oは酸素原子、Nは窒素原子)。
注3)励起:
分子等が外部からエネルギーを吸収して、より高いエネルギー状態になること。光子を吸収して励起する場合は光励起という。
注4)ラジカル:
通常、分子を構成する電子は2つずつ対になって存在しているが(この状態が安定、全体として偶数の電子)、特定の条件下では不対電子(1つの電子、全体として奇数の電子)で存在する場合がある。この状態にある分子をラジカルと呼び、アミド窒素上に不対電子があるものをアミジルラジカル、炭素原子上に不対電子があるものを炭素ラジカルと呼ぶ。
注5)結合解離エネルギー:
化学結合の強度の目安の1つであり、ある結合が 0 K (ケルビン)において均等開裂し2つのラジカルに分かれる場合の標準エンタルピー変化で定義される。
注6)光レドックス触媒:
光エネルギーを吸収して反応基質との電子の授受が可能になる触媒。
Information
| 論文タイトル | Zwitterionic Acridinium Amidate: A Nitrogen-Centered Radical Catalyst for Photoinduced Direct Hydrogen Atom Transfer |
|---|---|
| 著者 | Lukas-Maximilian Entgelmeier、森 宗一郎、仙頭 志音、山口 理恵、鈴木 隆平、柳井 毅*、Olga García Mancheño*、大松 亨介*、大井 貴史* (*は責任著者、下線は本学関係者) |
| 雑誌名 | Angewandte Chemie International Edition |
| DOI | 10.1002/anie.202404890 |
| 発行年月 | 2024年6月 |
